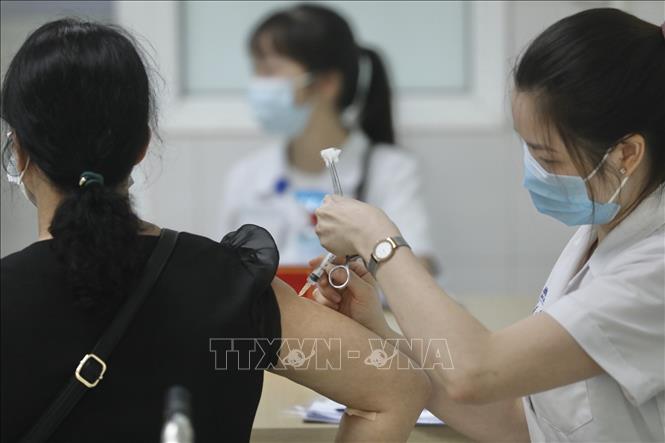
 Tiêm thử nghiệm vaccine Nano Covax. Ảnh: TTXVN
Tiêm thử nghiệm vaccine Nano Covax. Ảnh: TTXVN
Đại diện Hội đồng đạo đức trong nghiên cứu y sinh học Quốc gia vừa xác nhận vaccine Nano Covax (của Công ty Nanogen) đã được họp thẩm định kết quả giai đoạn 3a, bao gồm tính sinh miễn dịch, bổ sung, kết quả bước đầu giai đoạn 3b; kết luận đã đạt yêu cầu về an toàn và tính sinh miễn dịch.
Theo đó, Hội đồng chuyên môn sẽ sớm có thông tin chính thức về kết quả cuộc họp này.
Được biết, toàn bộ hồ sơ, dữ liệu của vaccine Nano Covax đã được chuyển sang Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, Bộ Y tế để tiếp tục xem xét trước khi trình Bộ Y tế đề xuất cấp phép khẩn cấp.
Đây là lần thứ hai Hội đồng Đạo đức họp thẩm định kết quả thử nghiệm lâm sàng vaccine Nano Covax giai đoạn 3.
Trước đó, Hội đồng Đạo đức đã chấp thuận kết quả thử nghiệm lâm sàng giai đoạn 3a đối với vaccine Nano Covax.