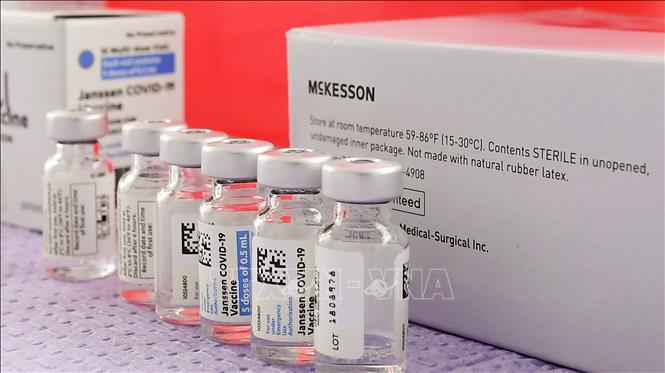
 Vaccine ngừa COVID-19 của hãng Johnson & Johnson. Ảnh: AFP/TTXVN
Vaccine ngừa COVID-19 của hãng Johnson & Johnson. Ảnh: AFP/TTXVN
Trong thông báo, nhà máy Emergent BioSolutions xác nhận FDA đã yêu cầu tạm dừng sản xuất vào ngày 16/4 vừa qua đối với loại vaccine một mũi của Johnson & Johnson. Theo yêu cầu của FDA, Emergent BioSolutions đã dừng việc sản xuất các nguyên liệu mới, cách ly lô hàng đã sản xuất tại cơ sở Bayview, ở thành phố Baltimore, thuộc bang Maryland cho đến khi hoàn tất quá trình điều tra.
Nhà máy Emergent BioSolutions ở Baltimore là nơi xảy ra sự cố nhầm lẫn thành phần vaccine của Johnson & Johnson và AstraZeneca khiến 15 triệu liều vaccine bị hỏng. Để tránh lặp lại sơ suất, Mỹ quyết định cho phép nhà máy chỉ sản xuất 1 loại vaccine của Johnson & Johnson. Tháng 3 vừa qua, Johnson & Johnson đã cử thêm chuyên gia đến nhà máy để giám sát công tác sản xuất vaccine và dự kiến sẽ cung cấp thêm 24 triệu liều vaccine trong tháng 4 này. Tuy nhiên, nhà máy Emergent BioSolutions tuyên bố chưa được nhà chức trách Mỹ cho phép sản xuất nguyên liệu bào chế vaccine của Johnson & Johnson.
Động thái trên là bước thụt lùi nữa trong chiến dịch tiêm phòng tại Mỹ, trong bối cảnh chính quyền đang tạm ngưng sử dụng vaccine của Johnson & Johnson sau khi ghi nhận 6 trường hợp bị đông máu, trong đó có 1 ca tử vong, sau khi tiêm phòng.
Mỹ dự kiến sẽ công bố quyết định có nối lại sử dụng vaccine của Johnson & Johnson hay không vào ngày 21/4. Trong khi đó, sau khi đánh giá 4 trường hợp bị đông máu sau tiêm, Cơ quan Dược phẩm của Liên minh châu Âu (EMA) cũng sẽ đưa ra quyết định về độ an toàn của vaccine do Johnson & Johnson bào chế trong cuộc họp báo ngày 20/4.
Trước đó, EMA nhận định các trường hợp đông máu là quá ít so với con số 4,5 triệu người đã tiêm phòng vaccine của Johnson & Johnson trên toàn thế giới. Cùng chung quan điểm này, Giám đốc Viện Dị ứng và Bệnh truyền nhiễm quốc gia Mỹ, Tiến sĩ Anthony Fauci đánh giá đây là hiện tượng vô cùng hiếm, đồng thời cho rằng Mỹ nên nối lại việc sử dụng vaccine của Johnson & Johnson, kèm theo một số hạn chế hay cảnh báo.
Trong diễn biến khác, Bộ Ngoại giao Mỹ thông báo đến ngày 18/4, chính quyền đã chuyển vaccine ngừa COVID-19 cho toàn bộ các nhân viên nước ngoài.
Đầu năm nay, Bộ Ngoại giao Mỹ đã hứng chịu nhiều chỉ trích khi gặp khó khăn trong việc tiêm phòng cho hàng nghìn nhân viên ngoại giao đang làm việc tại 220 địa điểm ở nước ngoài. Các quan chức bộ này sau đó đã thừa nhận đang bị thiếu nguồn cung vaccine.
Trong bối cảnh chương trình tiêm phòng trong nước diễn ra nhanh chóng, nguồn cung vaccine cho các nhân viên của Bộ Ngoại giao Mỹ ở nước ngoài cũng được đáp ứng đầy đủ. Một quan chức giấu tiên của bộ này xác nhận trong 3 đến 4 tuần tới, các nhân viên sẽ được tiêm phòng vaccine của hãng Pfizer hoặc Moderna và chương trình tiêm phòng sẽ hoàn tất vào giữa tháng 5.
Tính đến ngày 19/4, Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Mỹ (CDC) đã sử dụng hơn 211 triệu liều vaccine. Ước tính hơn 85 triệu người đã được tiêm đủ số mũi cần thiết.
* Tại Áo, nước này cho biết đang lên kế hoạch đến tháng 8, có thể cung cấp 651.000 liều vaccine của Pfizer/BioNTech cho các quốc gia tại vùng Tây Balkan trong khuôn khổ chương trình hỗ trợ của Liên minh châu Âu (EU) tới các nước láng giềng và châu Phi.
Tháng 1 vừa qua, Ủy ban châu Âu (EC) đã công bố kế hoạch triển khai chương trình chia sẻ vaccine. Áo đã nhận trách nhiệm là bên điều phối chia sẻ vaccine cho các nước ở vùng Tây Balkan. Phát biểu tại họp báo, Ngoại trưởng Áo Alexander Schallenberg khẳng định số vaccine này không nằm trong chương trình tiêm phòng quốc gia, mà là số hàng EU công khai dành cho các đối tác. Dự kiến số vaccine này sẽ phân phối từ đầu tháng 5 tới những nước cần nhất. Bosnia và Herzegovina sẽ nhận được 214.000 liều vaccine, tiếp đó là Albania (145.000 liều), CH Bắc Macedonia (119.000 liều) và Serbia (36.000 liều).