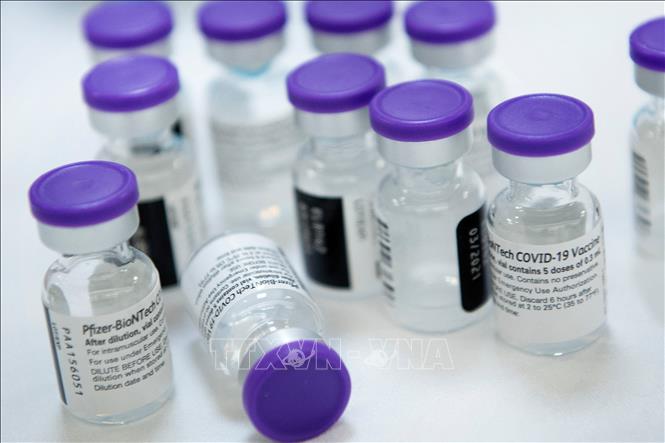
 Vaccine ngừa COVID-19 của Hãng Pfizer tại Falls Church, bang Virginia (Mỹ). Ảnh tư liệu: AFP/TTXVN
Vaccine ngừa COVID-19 của Hãng Pfizer tại Falls Church, bang Virginia (Mỹ). Ảnh tư liệu: AFP/TTXVN
Tuyên bố của EMA nêu rõ, quyết định của cơ quan này sẽ chủ yếu dựa vào kết quả đánh giá, dự kiến sẽ có vào tháng 6, trừ khi cần thêm thông tin bổ sung.
Trước đó, ngày 30/4, hai hãng dược phẩm Pfizer (Mỹ) và BioNTech (Đức) đã đề nghị EMA cấp phép sử dụng vaccine do hai hãng này phối hợp phát triển cho nhóm đối tượng từ 12 - 15 tuổi. Pfizer và BioNTech cam kết sẽ có đủ vaccine cung cấp cho nhóm đối tượng này từ tháng 6 tới. Hiện hai hãng này cũng đang có kế hoạch đưa ra đề nghị tương tự với cơ quan quản lý dược phẩm ở các nước khác trong những ngày tới.
Tháng 3 vừa qua, Pfizer và BioNTech khẳng định, trong giai đoạn 3 thử nghiệm lâm sàng, vaccine do hai hãng phối hợp bào chế đã chứng tỏ hiệu quả 100% trong việc phòng ngừa virus SARS-CoV-2 đối với trẻ em từ 12-15 tuổi và tạo kháng thể mạnh. Tuy nhiên, hiện vaccine Pfizer/BioNTech mới chỉ được cấp phép sử dụng cho người từ 16 tuổi trở lên.