 Katalin Kariko là một trong những người tiên phong với công nghệ mRNA, công nghệ được Pfizer/BioNTech và Moderna sử dụng để sản xuất vaccine phòng COVID-19. Ảnh: NYT
Katalin Kariko là một trong những người tiên phong với công nghệ mRNA, công nghệ được Pfizer/BioNTech và Moderna sử dụng để sản xuất vaccine phòng COVID-19. Ảnh: NYT
Nhờ những chiến dịch tiêm chủng quy mô lớn, hy vọng thoát khỏi đại dịch COVID-19 của nhân loại đang đến gần. Nhưng ít người biết rằng, đằng sau thành công của hai loại vaccine do Pfizer và Moderna sản xuất, là nhà khoa học nữ người Mỹ gốc Hungary, người đã tận tuỵ và hy sinh trong suốt 30 năm để mở đường cho công nghệ mRNA. Bà là Katalin Kariko.
Đó là câu chuyện về một nhà khoa học đã đấu tranh, chịu đựng và không chịu từ bỏ, bất chấp bị chê cười, mất việc và mắc bệnh ung thư. Suốt sự nghiệp của mình, Tiến sĩ Kariko đã tập trung vào RNA thông tin, hay mRNA - tập lệnh di truyền mang các chỉ dẫn DNA đến bộ máy tạo ra protein của mỗi tế bào. Bà tin rằng mRNA có thể được sử dụng để hướng dẫn các tế bào sản xuất “thuốc” của riêng chúng, bao gồm cả vaccine.
Nhưng Kariko đã trải qua phần lớn sự nghiệp của mình đối phó với những lời từ chối! Công việc của bà – nỗ lực khai thác sức mạnh của mRNA để chống lại bệnh tật, trong một thời gian dài đã bị coi là viển vông, bị chính phủ và các công ty khước từ bất kỳ khoản tài trợ nào, thậm chí cả sự ủng hộ từ các đồng nghiệp cũng không có. Là một nhà khoa học bị “hắt hủi”, Kariko chưa bao giờ kiếm được hơn 60.000 USD một năm.
Còn giờ đây ở tuổi 66, Katalin Kariko nổi lên như một trong những vị "anh hùng" của công cuộc phát triển vaccine COVID-19 công nghệ mRNA. Nghiên cứu của bà, với sự cộng tác của Tiến sĩ Drew Weissman tại Đại học Pennsylvania, đã đặt nền móng cho hai loại vaccine thành công tuyệt vời do Pfizer/BioNTech và Moderna sản xuất.
 Katalin Karik�o, hiện là Phó chủ tịch cấp cao tại BioNTech phụ trách mảng mRNA. Ảnh: Boston Globe
Katalin Karik�o, hiện là Phó chủ tịch cấp cao tại BioNTech phụ trách mảng mRNA. Ảnh: Boston Globe
"Vị thần" bị cười nhạo
Sinh năm 1955, Kariko là con gái một người bán thịt ở thị trấn nhỏ Kisujszallas, Hungary. Say mê khoa học từ khi còn trẻ, Kariko lấy bằng Tiến sĩ tại Đại học Szeged và làm nghiên cứu sinh sau tiến sĩ tại Trung tâm Nghiên cứu Sinh học của trường. Năm 1985, khi chương trình nghiên cứu của trường đại học hết kinh phí, Kariko cùng chồng và con gái 2 tuổi chuyển đến Mỹ làm nghiên cứu sinh sau tiến sĩ tại Đại học Temple ở Philadelphia.
Năm 1989, bà nhận một vị trí cấp thấp là trợ lý giáo sư nghiên cứu tại Đại học Pennsylvania, làm việc với Tiến sĩ Elliot Barnathan, một bác sĩ tim mạch.
Kariko và Tiến sĩ Barnathan đã lên kế hoạch chèn mRNA vào các tế bào, khiến chúng tạo ra các protein mới. Ở một trong những thí nghiệm đầu tiên, họ hy vọng sử dụng chiến lược này để hướng dẫn các tế bào tạo ra một loại protein được gọi là thụ thể urokinase. Nếu thí nghiệm có kết quả, họ sẽ phát hiện ra protein mới nhờ một phân tử phóng xạ sẽ được thu hút đến thụ thể.
“Hầu hết mọi người đều cười nhạo chúng tôi", Tiến sĩ Barnathan kể lại.
Một ngày định mệnh, hai nhà khoa học đi lại quanh chiếc máy in kim ở cuối hành lang. Một máy đếm gamma, công cụ cần thiết để theo dõi phân tử phóng xạ, được gắn vào máy in, và nó bắt đầu cho ra dữ liệu. Máy dò của họ đã tìm thấy các protein mới được tạo ra bởi những tế bào lẽ ra không bao giờ có thể tạo ra chúng – điều đó cho thấy mRNA có thể được sử dụng để chỉ đạo bất kỳ tế bào nào tạo ra bất kỳ loại protein nào theo ý muốn.
“Tôi cảm thấy mình như một vị thần vậy!”, Tiến sĩ Kariko nhớ lại khoảnh khắc đó.
 Tiến sĩ Kariko và gia đình vào năm 1985. Ảnh: NYT
Tiến sĩ Kariko và gia đình vào năm 1985. Ảnh: NYT
Kariko và Tiến sĩ Barnathan đã nghĩ đến ý tưởng sử dụng mRNA để cải thiện mạch máu cho phẫu thuật tim đường vòng. Họ thậm chí có thể sử dụng quy trình này để kéo dài tuổi thọ của tế bào người.
Nhưng giữa lúc thành công bước đầu, Tiến sĩ Barnathan lại rời trường đại học, làm việc cho một công ty công nghệ sinh học, bỏ lại cộng sự Kariko chơ vơ không có phòng thí nghiệm và cả hỗ trợ tài chính.
May mắn thay, một đồng nghiệp khác đã tin tưởng vào bà: Tiến sĩ David Langer, một bác sĩ giải phẫu thần kinh, người đã thúc giục trưởng khoa phẫu thuật thần kinh trao cơ hội nghiên cứu cho Kariko. Nhưng Langer cuối cùng cũng rời trường đại học, một lần nữa để lại Kariko “tay trắng”.
Bị sa thải, không tiền bạc, mắc bệnh ung thư
Đến năm 1995, 10 năm sau khi đến Mỹ, Kariko bị sa thải khỏi Đại học Pennsylvania và sau đó bị chẩn đoán mắc bệnh ung thư. Không còn tiền để hỗ trợ công việc nghiên cứu mRNA, bà chấp nhận trở lại với một vị trí thấp hơn tại Viện hàn lâm khoa học.
Tại đây, chính cuộc gặp gỡ định mệnh của Kariko với bác sĩ miễn dịch học Drew Weissman, người đang nghiên cứu vaccine HIV, vào cuối những năm 1990 đã thúc đẩy sự nghiệp của bà.
Bộ đôi bắt đầu hợp tác và xin tài trợ, nhưng không mấy may mắn. Weissman nói: "Chúng tôi hầu như không nhận được tiền. Mọi người không quan tâm đến mRNA. Những người xem xét tài trợ cho biết mRNA sẽ không phải là một liệu pháp tốt, vì vậy đừng bận tâm".
 Kariko cho biết, bà "hạnh phúc trong phòng thí nghiệm".
Kariko cho biết, bà "hạnh phúc trong phòng thí nghiệm".
Các tạp chí khoa học hàng đầu cũng từ chối công trình của họ. Khi nghiên cứu cuối cùng được công bố, nó không được mấy người chú ý. "Vào thời điểm đó, mọi người chỉ nói tạm biệt và bỏ đi vì nó quá kinh khủng", Kariko kể lại trong một cuộc phỏng vấn.
Nhưng bà vẫn kiên trì đối mặt với khó khăn. "Nhìn thì có vẻ điên rồ, chật vật, nhưng tôi thấy hạnh phúc trong phòng thí nghiệm", bà nói với Business Insider.
Năm 2005, Kariko và Weissman đã đạt được một bước đột phá lớn, cho phép mRNA tổng hợp vượt qua được hệ miễn dịch của cơ thể.
Trong nghiên cứu, họ đã chứng tỏ có thể khiến một con vật (con khỉ) tạo ra một loại protein mà họ đã chọn. Hai nhà nghiên cứu đã tiêm mRNA cho khỉ để hướng dẫn tạo ra erythropoietin, một loại protein kích thích cơ thể tạo ra các tế bào hồng cầu. Số lượng tế bào hồng cầu của con vật tăng vọt.
Hai nhà khoa học cho rằng phương pháp tương tự có thể được sử dụng để thúc đẩy cơ thể tạo ra bất kỳ loại “thuốc protein” nào, như insulin hay các hormone khác hoặc một số loại thuốc tiểu đường mới. Điều quan trọng, mRNA cũng có thể được sử dụng để tạo ra vaccine, không giống như bất kỳ loại vaccine xuất hiện trước đây.
Đột phá mở đường cho vaccine công nghệ mRNA
Công trình của họ đã thu hút sự chú ý của hai nhà khoa học chủ chốt. Một trong số họ là nhà sinh học tế bào gốc người Canada Derrick Rossi, người sau này đã giúp thành lập Moderna và đối tác tương lai của Pfizer, BioNTech. Rossi không chỉ công nhận đó là một bước đột phá mà giờ đây ông còn tin rằng Kariko và Weissman xứng đáng nhận giải Nobel Hóa học.
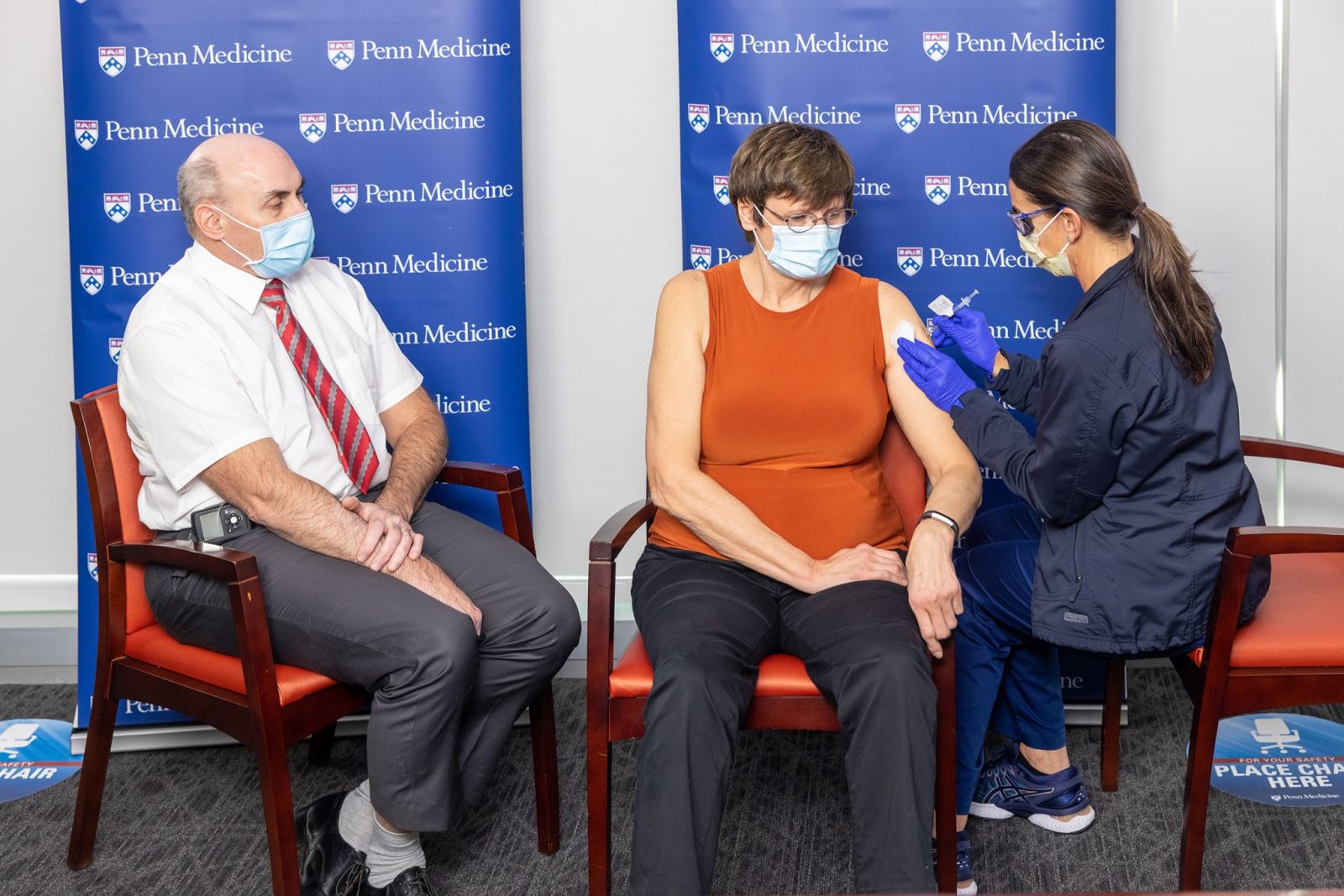 Tiến sĩ Kariko (giữa) và cộng sự Weissman được tiêm vaccine COVID-19. Ảnh: Hungarytoday
Tiến sĩ Kariko (giữa) và cộng sự Weissman được tiêm vaccine COVID-19. Ảnh: Hungarytoday
Vaccine được chia làm ba loại chính: Thứ nhất là vaccine truyền thống, sử dụng virus bất hoạt hoặc đã chết, độc tố của virus và protein hay các thành phần khác của virus để kích hoạt miễn nhiễm; Thứ hai là vaccine vector virus, sử dụng một loại virus an toàn để kích hoạt miễn nhiễm; Thứ ba vaccine dựa trên công nghệ mRNA. Vaccine công nghệ mRNA là mới nhất, sử dụng mRNA để vượt qua hệ miễn dịch của người và tạo ra các protein cụ thể kích hoạt miễn nhiễm.
So với công nghệ truyền thống, mRNA hứa hẹn hiệu quả hơn, nhanh hơn, an toàn hơn, ít tác dụng phụ hơn; có thể so sánh sự khác biệt giống như xe máy và chuyên cơ. Để dễ hiểu, có thể hình dung quá trình tổng hợp mỗi protein trong cơ thể con người giống như giải một bài toán phức tạp, mRNA trở thành cuốn sổ tay những công thức toán học. Nếu con người tạo ra được vaccine dưới dạng mRNA nhân tạo, khi tiêm vào cơ thể, mRNA sẽ nguỵ trang giống như “kẻ trộm” lẻn vào nhưng không đánh thức “chủ nhà”, nó âm thầm xây dựng một hệ thống phòng thủ là những protein kháng thể, để khi virus tấn công sẽ bị hệ thống ấy tiêu diệt.
Các nhà nghiên cứu tại Pfizer-BioNTech và Moderna đã sử dụng các kỹ thuật của Kariko và Weissman để phát triển vaccine của họ. Ý tưởng cho cả hai loại vaccine mà Moderna và BioNTech theo đuổi là đưa mRNA vào cơ thể để hướng dẫn các tế bào của con người sản xuất protein gai của SARS-CoV-2. Hệ miễn dịch sẽ nhìn thấy protein, nhận ra nó là kẻ lạ xâm nhập và học cách tấn công SARS-CoV-2 nếu nó xuất hiện trong cơ thể.
Vào ngày 8/11/2020, kết quả đầu tiên của nghiên cứu Pfizer/BioNTech đã được công bố, cho thấy vaccine mRNA cung cấp khả năng miễn dịch mạnh mẽ đối với virus SARS-CoV-2 gây COVID-19.
Công nghệ mRNA sẽ không dừng lại ở sản xuất vaccine, mà trong tương lai không xa, hàng loạt bệnh như ung thư, đột quỵ, hay các bệnh hiểm nghèo khác cũng hứa hẹn sẽ được “thanh toán”. Sau nhiều thập kỷ đứng ngoài rìa cộng đồng khoa học, Kariko và Weissman đang là những gương mặt tiềm năng của giải Nobel Y học năm 2021.